일론 머스크 효과? 美서 불어온 체중감량 열풍
국내 제약사, 당뇨치료제→비만치료 활용 속도
대규모 임상 진행 중…올해 안에 윤곽 나올 듯

제약업계가 비만치료제 개발에 뛰어들고 있다. 덴마크 제약사 노보노디스크가 비만치료제 ‘위고비’를 내놓으면서 국내 제약사들도 비만치료제 개발에 집중하고 있다. (CNB뉴스=김민영 기자)
비만치료제 시장의 판도를 바꾼 것은 당뇨병 치료제로 쓰였던 ‘GLP-1 수용체 작용제’다.
‘GLP-1 수용체 작용제’는 처음에 제2형 당뇨병 관리를 위해 개발됐다. 체중 감량에 대한 ‘GLP-1 수용체 작용제’의 역할이 나타났고, 당뇨병이 없는 사람도 비만 치료에 사용할 수 있도록 적응증이 확대됐다. 적응증이란 약으로 인해 치료효과가 기대되며, 확대라는 단어가 붙을 시 임상 등을 통해 치료가 가능한 병증이다는 의미다.
‘GLP-1’은 인체에서 자연적으로 생성되는 호르몬이다. 췌장에서 인슐린 분비를 촉진해 혈당을 떨어뜨린다. 이는 위 배출 속도를 지연시키고 식욕 억제를 일으키기 때문에 체중 감량에 도움이 된다.
‘GLP-1 수용체 작용제’는 ‘GLP-1’과 동일한 구조를 가진 약물이다. GLP-1 수용체에 결합해 GLP-1과 유사한 작용을 하는 것이 특징이다.
“단식 그리고 위고비(Fasting and Wegovy)”
지난해 10월 한 트위터 사용자가 테슬라 최고경영자 일론머스크에게 “군살이 없고 건강해 보이는데 비결이 무엇인가요?”라고 묻자 답한 말이다.
최근 미국에선 덴마크 제약업체 노보노디스크의 비만치료제 위고비 열풍이 거세다. 위고비는 애초 당뇨 치료제로 개발됐으나, 식욕 억제를 통한 체중 감량 효과가 부각되고, 비만치료제로써 관심을 받았다.
미국 테슬라의 최고경영자(CEO) 일론 머스크는 ‘위고비’ 약을 처방받았고, 유명 방송인인 오프라 윈프리는 ‘오젬픽’이라는 약을 이용해 체중 감량에 성공한 것으로 알려졌다.
한미약품, 개발 속도 가장 빨라
이에 국내 대표 제약사들도 비만치료제에 팔을 걷어붙이고 나섰다.
한미약품은 독자 플랫폼 기술인 ‘랩스커버리’가 적용된 당뇨병 치료제로 GLP-1계열 ‘에페글레나타이드’를 개발했다. ‘에페글레나타이드’는 한미약품이 독자 플랫폼 기술 ‘랩스커버리’를 적용해 일주일에 한번 투여하는 주사 제형이다. 프랑스 사노피에 기술 수출해 혁신성과 안전성 등을 입증받았지만, 파트너사 정책 등의 이유로 에페글레나타이드 기술을 다시 반환받았다.
이후 한미약품은 약물 개발 방향을 비만치료제로 재설정하고 비만 치료 프로젝트 ‘H.O.P(Hanmi Obesity Pieline)’를 전개하고 있다. H.O.P는 비만 예방, 치료, 체중 관리에 이르는 비만 전 주기 맞춤형 포트폴리오 구축 프로젝트다.
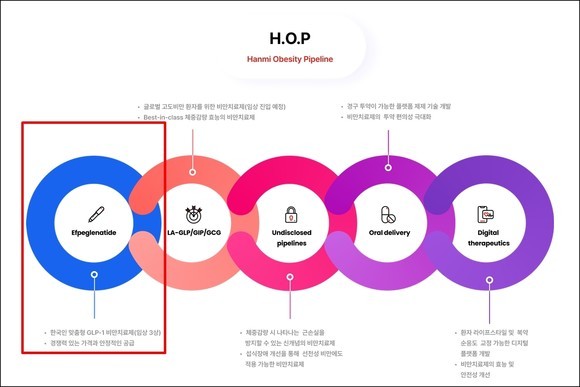
특히 당뇨병 치료제 관련 다양한 임상을 거치면서 안전성을 검증받았기 때문에 개발 속도는 국내 제약사 중 가장 빠른 편이다.
대규모 글로벌 임상 3상에서 체중감소와 혈당조절 효능을 확인했고 주요 심혈관계 및 신장 질환 발생률을 유의미하게 감소시키는 효능까지 임상 시험을 통해 검증했다. 해당 임상 결과는 세계적인 학술지인 뉴잉글랜드 저널 오브 메디슨(NEJM) 등 다수의 학술지에 해당 결과가 등재되기도 했다. 한미약품은 위고비와 마찬가지로 주 1회 투여 비만치료제 상용화를 목표로 설정한 상태다.
또한 한미약품은 국내 성인 비만 환자를 대상으로 ‘에페글레나타이드’의 유효성 및 안전성을 평가하는 임상 3상 시험에 참가할 첫 환자를 이달 초 등록했다. 앞서, 지난해 10월 식품의약품안전처로부터 임상 3상 계획을 승인받은 후 약 2개월 반 만에 이뤄진 결과다.
이후 순차적으로 임상 시험대상자는 점차 늘어난다. 국내 대학병원에서 당뇨병을 동반하지 않은 성인 비만 환자 420명을 대상으로 무작위 배정, 이중 눈가림, 위약 대조, 평행 비교 방식 등으로 진행될 전망이다. 임상 종료 시점은 오는 2026년 상반기로 예상하고 있다. 한미약품 측은 3년 내 국내 상용화를 기대하고 있다고 밝혔다.
적자 벗어난 일동제약, ‘먹는 치료제’ 속도
지난해 4분기 영업이익 흑자 전환을 기점으로 일동제약도 비만치료제 개발에 속도를 내고 있다.
일동제약 측은 자회사 유노비아가 개발하는 경구용 GLP-1(글루카곤유사펩타이드-1) 수용체 작용제 ‘ID110521156’의 임상 1상 결과가 상반기 내 나올 것으로 기대하고 있다. ID110521156은 체내에서 인슐린 분비를 유도해 혈당 수치를 조절하는 ‘GLP-1 호르몬’의 유사체로 작용한다. 지난해 9월 식품의약품안전처로부터 임상 1상 시험 계획(IND) 승인을 취득했다.
아울러 펩타이드 제제에 비해 구조적으로 안정적인 ‘ID110521156’의 특성을 활용해 제조 효율 및 생산성이 뛰어나고, 환자 입장에서 사용이 편리한 경구용(먹는) 치료제도 개발할 계획이다.
이밖에 동아에스티의 자회사 뉴로보 파마슈티컬스는 지난해 6월 미국 샌디에이고에서 열린 83회 미국 당뇨학회(ADA)에서 비만 신약 ‘DA-1726’의 체중 감소 효과 결과를 발표했다. DA-1726은 식욕 억제 및 인슐린 분비 촉진, 말초에서 기초대사량을 증가시켜 체중감소와 혈당조절을 유도한다.
최근 동아에스티는 지난달에 ‘DA-1726’ 1상 미국식품의약국(FDA) 1상 임상시험계획(IND)을 제출한 바 있다. FDA는 제출된 임상시험계획서를 검토한 후 임상 진행 여부를 결정하기로 했으며, 뉴로보는 올해 상반기 임상 1상을 시작해 내년 상반기에 1상을 마칠 것으로 기대하고 있다.
(CNB뉴스=김민영 기자)



















![[생생르포] ‘열린 공장’을 체험하다…평택 ‘hy팩토리+’ 가보니](https://www.cnbnews.com/data/cache/public/photos/cdn/20260207/art_1770878463_176x135.jpg)


















































