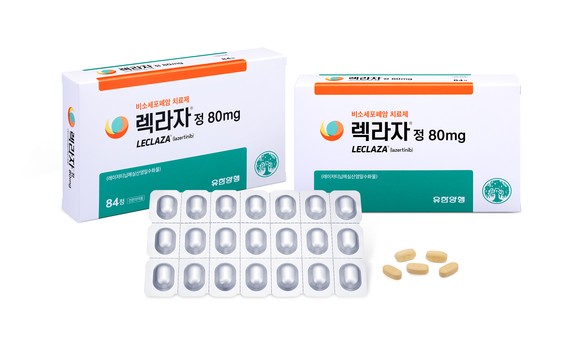
유한양행이 개발한 폐암치료제 ‘렉라자’(성분명 레이저티닙)가 1차 치료제로 보험급여가 확대된다.
27일 유한양행에 따르면, 상피세포 성장인자 수용체(EGFR) 돌연변이 양성 비소세포폐암 치료제 렉라자가 내년 1월 1일부터 1차 치료에서 건강보험 급여가 적용될 예정이다. 렉라자의 1차 치료 급여 확대로 EGFR 엑손 19 결손 또는 엑손 21(L858R) 치환 변이된 국소 진행성 및 전이성 비소세포폐암 환자의 1차 치료도 급여 처방이 가능해졌다.
기존 급여 범위였던 이전에 상피세포 성장인자 수용체 티로신 키나제 억제제(EGFR-TKI) 투여 후 질병 진행이 확인된 T790M 변이 양성 국소 진행성 또는 전이성 환자 치료 시 2차 약제까지 포함하면 1·2차 치료 단계에서 모두 급여 혜택을 받을 수 있게 됐다.
이번 급여 적용은 LASER301 임상 3상 시험에서 확인된 EGFR 변이 비소세포폐암 1차 치료에 대한 임상적 유효성을 토대로 이뤄졌다. LASER301 임상은 이전에 치료를 받은 적이 없는 활성 EGFR 돌연변이 양성 국소 진행성 또는 전이성 비소세포폐암 393명(아시아인 258명, 비아시아인 135명)을 대상으로 실시했다. 게피티니브 투여 대비 렉라자 투여 유효성과 안전성을 평가한 무작위배정, 이중눈가림, 다국가 3상 임상시험이다.
임상 결과 렉라자 투여군은 1차 평가변수인 시험자 평가 기반 무진행 생존기간(PFS) 중앙값을 20.6개월로 달성했다. 대조군 게피티니브 투여군의 9.7개월보다 통계적으로 유의미하게 PFS를 개선했다.
아시아인 하위그룹 분석에서 렉라자 투여군의 PFS 중앙값은 20.6개월로 달성했다. 게피티니브 투여군은 9.7개월로 역시 통계적으로 유의미한 개선을 보였다.
중추신경계(CNS) 전이 여부에 따른 하위 그룹 분석 결과에서는 CNS 전이가 있는 환자군에서는 PFS 중앙값은 렉라자 투여군 16.4개월, 게피티니브 투여군 9.5개월로 나타났다. CNS 전이가 없는 환자군에서는 렉라자 투여군 20.8개월, 게피티니브 투여군 10.9개월로 나타나 치료 예후가 좋지 않은 CNS 전이가 있는 환자군에서도 우수한 항종양 효과를 입증했다.
조욱제 유한양행 사장은 “암사망률 1위 폐암 중에서 한국인에 흔한 EGFR 변이 비소세포폐암 치료에서 새로운 치료 옵션인 유한양행 렉라자가 1차 치료 급여 확대로 환자분들의 치료 접근성이 개선돼 매우 기쁘다”면서 “혁신 신약 개발과 치료 접근성 향상을 위해 계속 힘쓰겠다”고 말했다.



















![[생생르포] ‘열린 공장’을 체험하다…평택 ‘hy팩토리+’ 가보니](https://www.cnbnews.com/data/cache/public/photos/cdn/20260207/art_1770878463_176x135.jpg)


















































